Amazon輸出で販売規制対象となりハードルが高いFDA登録が必要な商品の登録方法についてまとめました。
輸入ビジネスでは食品衛生法の許可を取ったり電気用品安全法の許可を取るテクニックは当たり前になっていますが輸出ではなぜか一部のセラーしか行なっていない印象です。
FDA登録とは
FDAとはアメリカ食品医薬品局(Food and Drug Administration)のことでFDA登録とは米国への輸入や米国での販売に許認可が必要な商品の許認可登録をすることです。
日本では食品については、所轄行政官庁が厚生労働省以外にも複数の官庁(農林水産省、経済産業省など)に渡りますがアメリカではFDAで一元的に管理されています。
一元的に管理されるとされていますすが実態としては7センター(CBER、CDER、 CDRH、CFSAN、CTP 、CVM、NCTR)および ORA に分かれています。
FDA登録が必要な代表的な商品事例
- 食品
- 医薬品
- 化粧品
医薬品
日本では化粧品として扱われている製品でも、内容成分や効果効能等の表示内容によっては、FDAによって医薬品とみなされる場合がある点に注意しましょう。
日焼け止めや薬用シャンプーなどは成分によっては医薬品規制の対象になることがあります。
化粧品
化粧品(Cosmetic)はアメリカの連邦食品・医薬品・化粧品法(Federal Food, Drug and Cosmetic Act: FDCA)により「人の体に塗る、馴染ませる、スプレーする等により、体をきれいに美しくし、魅力を高め、または外見を変えるためのもの」と定義されています。
また保湿剤やシャンプーのほか、練り歯磨き粉も化粧品に分類されます。
ちなみに食品や医薬品と異なりFDAへの化粧品登録は義務ではありません。
しかし化粧品製造業者、梱包業者、配送業者は市場流通後に化粧品自主登録プログラム (Voluntary Cosmetic Registration Program (VCRP))への自主登録が推奨されており同プログラムへ登録することで、FDAのデー タベースに化粧品成分内容が登録される事で安全性を判断する化粧品科学者団体 (Cosmetic Ingredient Review (CIR))に研究されるため、ブランディング効果があります。
FDA登録の方法
FDA登録をしたければFDAのエージェントに依頼しましょう、と言ってしまえばそれで終了になってしまうのでFDA登録の流れを解説します。
日本の薬事法などを通す時と一緒で商品によって審査難度が異なるので医薬品など難しいものは専門業者に任せて日本で言う食品衛生法関係の簡単なものは自分で通せるようになるのがベストだと思います。
なお個人でやる場合も米国の代理人が必要になります。米国の代理人は専門家である必要はありませんが緊急事態が発生した時にFDAが連絡を取る役割の人でアメリカ国内にビジネス拠点または居住場所を持つ人である必要があります。
個人で輸出するときにアメリカに住所のあるインポーターを立てる必要があるのと同じです。
またFDA登録を通すには必要事項のラベルの英語表記を行う必要があるので事前に準備しておきましょう。
これらを踏まえた上でFDA登録の方法を見ていきたいと思います。
アカウントの作成
FDAのHPからアカウント作成を行います。Create Accountからアカウントを作成しましょう。
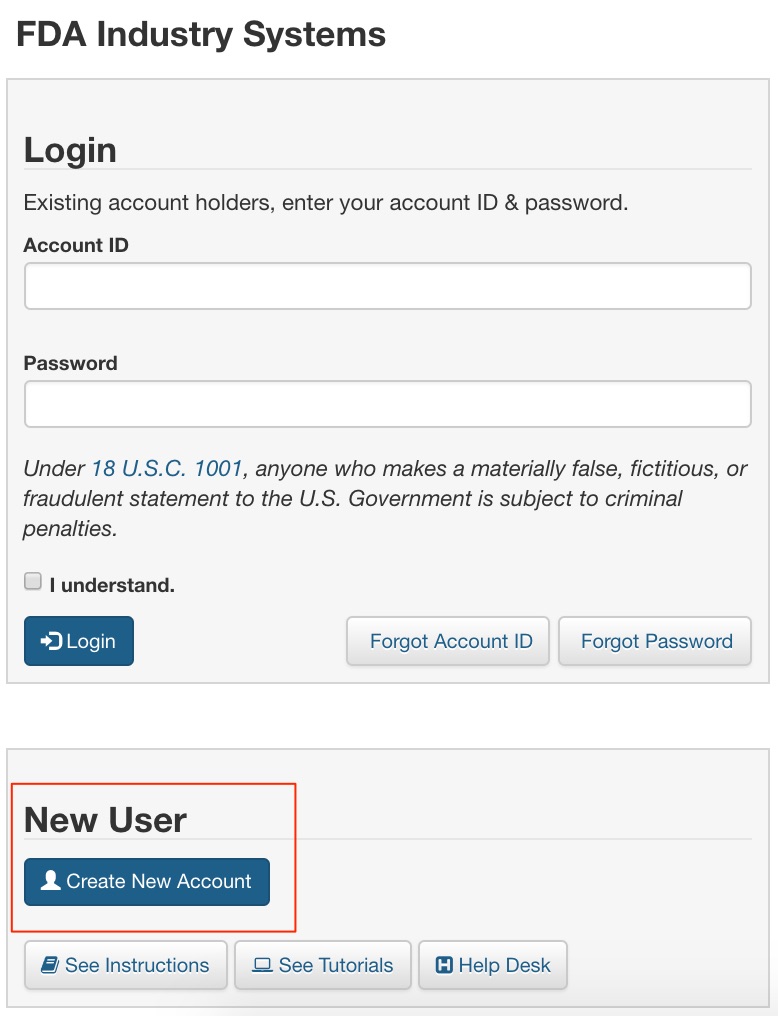
次に必要事項を入力していきます。
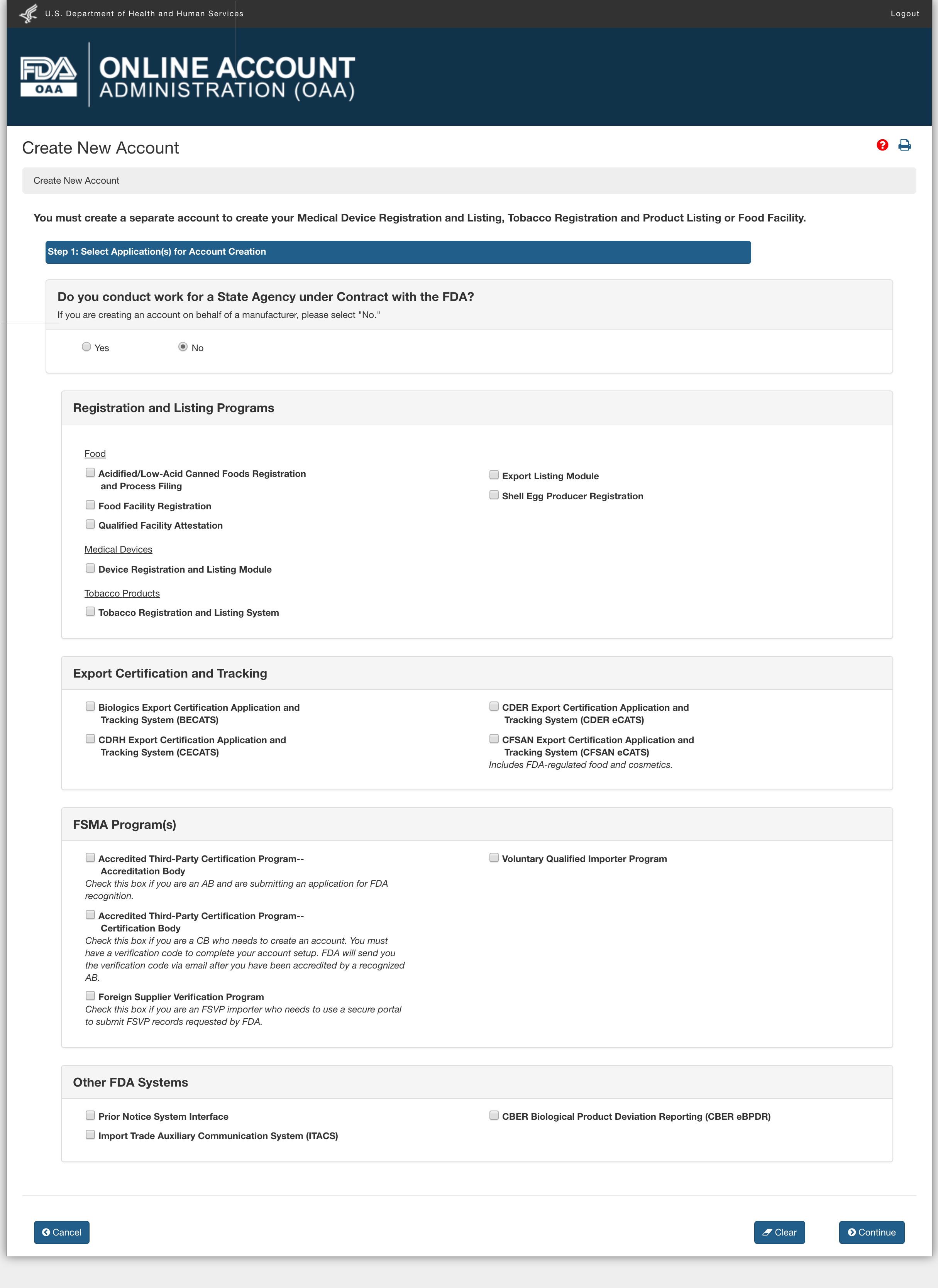
最初の質問はFDA AgentであるかどうかなのでNoを選択。
Registration and Listing Programs
Registration and Listing Programsは申請する商品や機器、施設に応じて以下のものから選択します。
Food
- Acidified/Low-Acid Canned Foods Registration and Process Filing
- Food Facility Registration
- Qualified Facility Attestation
- Export Listing Module
- Shell Egg Producer Registration
Medical Devices
Device Registration and Listing Module
Tobacco Products
Tobacco Registration and Listing System
日本の食品を輸出したいような場合はFood Facility Registrationを選択することになります。
食品自体を登録するのではなく食品の製造場所を登録する必要があるのです。
Export Certification and Tracking
Export Certification and Trackingでは輸出証明書の認証を得る機関を選択します。
- CBER(BECATS) 生物医薬品局
- CDRH(CECATS) 医療機器·放射線保健センター
- CDER(CDER eCATS) 医薬品評価研究センター
- CFSAN(CFSAN eCATS) 食品安全・応用栄養センター
食品の場合は一番下のCFSAN(CFSAN eCATS)を選択します。
FSMA Program(s)
FSMAとは食品安全強化法のことでFSMA Programとは任意で参加した輸入業者のための食品輸入の手続き迅速化プログラムを意味します。
- Accredited Third-Party Certification Program– Accreditation Body
- Accredited Third-Party Certification Program– Certification Body
- Foreign Supplier Verification Program
- Voluntary Qualified Importer Program
外国サプライヤーである私たちは一番下のVQIPプログラムの下で食品の迅速な輸入に申請する輸入者に対する前提条件であるFSMA VQIP認証に申請することができます。
Other FDA Systems
FDA関連で使用したいシステムにチェックを入れます。
- Prior Notice System Interface FDA 事前通告システム・インターフェース
- Import Trade Auxiliary Communication System (ITACS) 国際貿易補助通信システム
- CBER Biological Product Deviation Reporting (CBER eBPDR) CBERバイオ製品逸脱報告
アメリカに輸出するヒトおよびその他の動物用の食品はFDAに事前通知することが必要になので一番上の事前通告システム・インターフェースにチェックを入れ輸出時にはFDAのHP上のシステムからアクセスし、必要な情報をオンライン上で登録した上で、FDAからPN確認番号を取得する必要があります。
FDA申請の方法
アカウント登録が終わったら実際の申請に進むわけですが以下のような流れになります。
- 製造施設の登録
- 米国代理人の指定
- 商品ラベルの英語化
- 食品安全計画の策定
- 事前通知
製造施設の登録はすでにアカウント登録の所で済ませていると思います。
米国代理人についても解説済みですね。
代理人は緊急事態が発生した時にFDAが連絡を取る役割の人でアメリカ国内にビジネス拠点または居住場所を持つ人である必要があります。
商品ラベルの英語化や食品安全計画の策定に関しては商品ジャンルごとに記入方法が微妙に異なるのでエージェントに相談するべきですがジェトロが事例を公開してくれているのでそちらを参照するのがおすすめです。
参照:食品安全計画の記入例
事前通知に関してはPrior Notice System Interface FDAを通してオンラインで行います。
どうでしょうか、自分で出来ないこともないと思いますが単純に作業量が結構多いので結局の所エージェントに任せてしまった方がいいかもしれませんがエージェントに任せるとしても今回紹介した内容を知っているのと知らないのとでは大違いなのでぜひこの機会にFDA登録について詳しく学んでみてください。
Amazon輸出のFDA登録の方法まとめ
いかがだったでしょうか輸入ビジネスでは参入者が増え販売規制がある商品を扱うか独占販売権を取得して販売するかOEMを行なっているセラー以外稼げなくなっているように輸出ビジネスでも一工夫しないと今までのように利益を出すのが難しい時代になっています。
日本のAmazonで食品販売をされている方などは特にFDAの規制対象の商品販売も1つの戦略として活用してみてはいかがでしょうか?
またここでは明かしませんがFDA登録が必要そうで実は必要のない商品というのは一般セラーが避けやすい商品である為狙い目です。ぜひ探してみてください。